Funcionarios de salud del gobierno estadounidense aprobaron el lunes el primer medicamento nuevo para la enfermedad de Alzheimer en casi 20 años, sin tener en cuenta las advertencias de asesores independientes de que no se ha demostrado que el tratamiento tan debatido ayude a retrasar la enfermedad que destruye el cerebro.
La Administración de Drogas y Alimentos de EE. UU. dijo que otorgó la aprobación al medicamento de Biogen basándose en resultados que parecían "razonablemente probables" para beneficiar a los pacientes con Alzheimer.
FDA approves the first treatment directed at the underlying biology of Alzheimer’s disease, which is expected to reduce the clinical decline of patients with this disease: https://t.co/xEVvn7V2Fi pic.twitter.com/OaADO8DkZB
— U.S. FDA (@US_FDA) June 7, 2021
Una aprobación controvertida
Este es el único medicamento que los reguladores estadounidenses han dicho que probablemente puede tratar la enfermedad subyacente. Normalmente se ocupan medicamentos para controlar síntomas como la ansiedad y el insomnio.
La decisión, que podría afectar a millones de estadounidenses mayores y sus familias, seguramente provocará desacuerdos entre médicos, investigadores médicos y grupos de pacientes. También tiene implicaciones de gran alcance para los estándares utilizados para evaluar terapias experimentales, incluidas aquellas que muestran solo beneficios incrementales.
El nuevo fármaco, que Biogen desarrolló con la compañía japonesa Eisai Co., no revirtió el declive mental, solo lo ralentizó en un estudio. El medicamento, Aducanumab, se comercializará como Aduhelm y se administrará en forma de infusión cada cuatro semanas.
El Dr. Caleb Alexander, un asesor de la FDA que recomendó no aprobar el medicamento, dijo que estaba "sorprendido y decepcionado" por la decisión.
“La FDA recibe el respeto que tiene porque tiene estándares regulatorios que se basan en pruebas firmes. En este caso, creo que aprobaron el producto ”, afirmó Alexander, investigador de la Universidad Johns Hopkins.
¿Una buena medida?
El principal regulador de medicamentos de la FDA reconoció en un comunicado que "incertidumbres residuales" rodean al medicamento. Igualmente la asociación afirmó que "se espera" que la capacidad de Aduhelm para reducir los grupos dañinos de placa en el cerebro ayude a retrasar la demencia.
Según los términos de la denominada aprobación acelerada, la FDA exige que el fabricante de medicamentos lleve a cabo un estudio de seguimiento para confirmar los beneficios para los pacientes. Si el estudio no muestra efectividad, la FDA podría retirar el medicamento del mercado, aunque la agencia rara vez lo hace.
Biogen no reveló el precio de inmediato, aunque los analistas han estimado que el medicamento podría costar entre $ 30,000 y $ 50,000 dólares por un año de tratamiento.
Un análisis preliminar realizado por un grupo encontró que el medicamento tendría que tener un precio de $ 2,500 a $ 8,300 por año para tener un buen valor basado en las “pequeñas ganancias generales para la salud” sugeridas por estudios de la compañía. La organización sin fines de lucro Institute for Clinical and Economic Review agregó que "cualquier precio es demasiado alto" si el beneficio del medicamento no se confirma en estudios de seguimiento.
Alzheimer: Una enfermedad sin cura
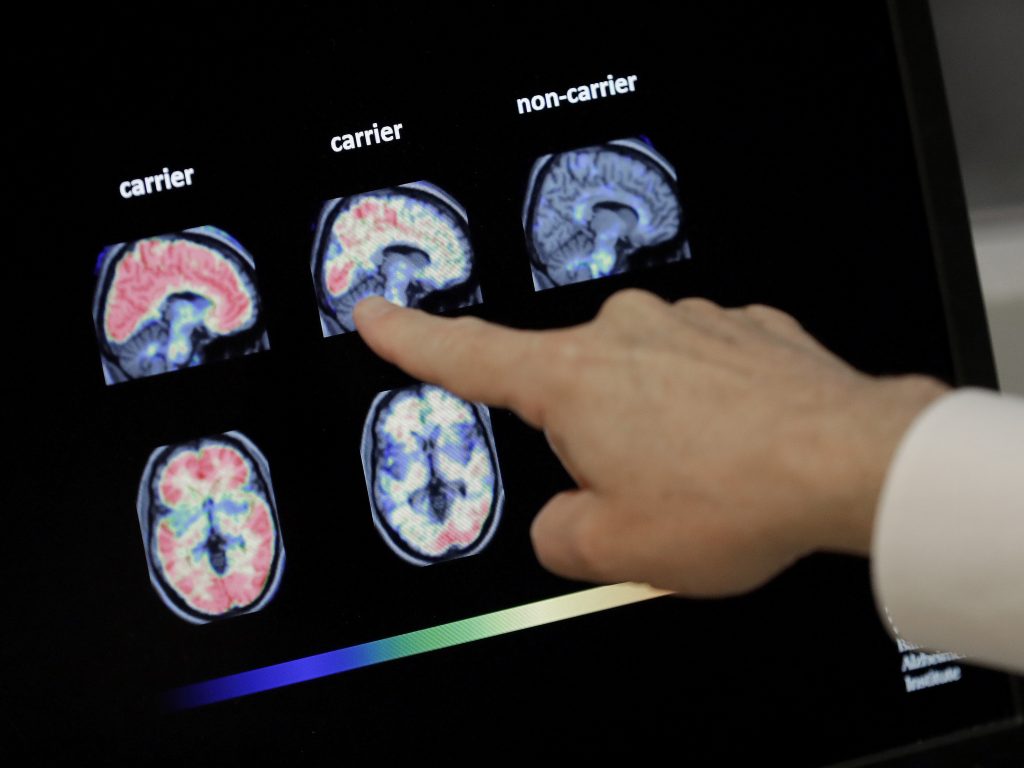
Casi 6 millones de personas en los EE. UU. y muchas más en todo el mundo tienen Alzheimer, que ataca gradualmente áreas del cerebro necesarias para la memoria, el razonamiento, la comunicación y las tareas diarias básicas. En las etapas finales de la enfermedad, los afectados pierden la capacidad de tragar. Solo se espera que la carga mundial de la enfermedad, la causa más común de demencia, aumente a medida que millones más de baby boomers avancen hacia los 60 y 70 años.
El Aducanumab ayuda a eliminar del cerebro una proteína relacionada con el Alzheimer, llamada beta-amiloide. Otros fármacos experimentales han hecho eso antes, pero no han marcado ninguna diferencia en la capacidad de los pacientes para pensar, cuidar de sí mismos o vivir de forma independiente.
La línea de medicamentos de la industria farmacéutica ha estado llena durante años de tratamientos fallidos para el Alzheimer. Es probable que la luz verde de la FDA reviva las inversiones en terapias similares previamente archivadas por los fabricantes de medicamentos.
El nuevo medicamento está elaborado a partir de células vivas que deberán administrarse mediante perfusión en el consultorio de un médico o en un hospital.
Sigue a Rockandpop.cl en Google Discover
Recibe nuestros contenidos directamente en tu feed.